皆さんは、
東京科学大院試に向けて過去問を解いているけど、難しい!
過去問の解答が欲しい!
と思っていませんか?
この記事では、2024年入学東京科学大の物質理工学院応用化学系の無機化学の問題解答について、解説していきます!
問題(Ⅱ-2)はこちら(ホームページ)からダウンロードできます。
ぜひ、問題を解いてから読んでみてください!
こちらの解答は正式なものではなく、筆者が出した解答ですのでその点には十分注意してお読みください!

Ⅱ-2(1)
①
ア 6
イ 12
②
面心立方格子
③
(a) $a = 2\left( {{r_B} + {r_O}} \right)$
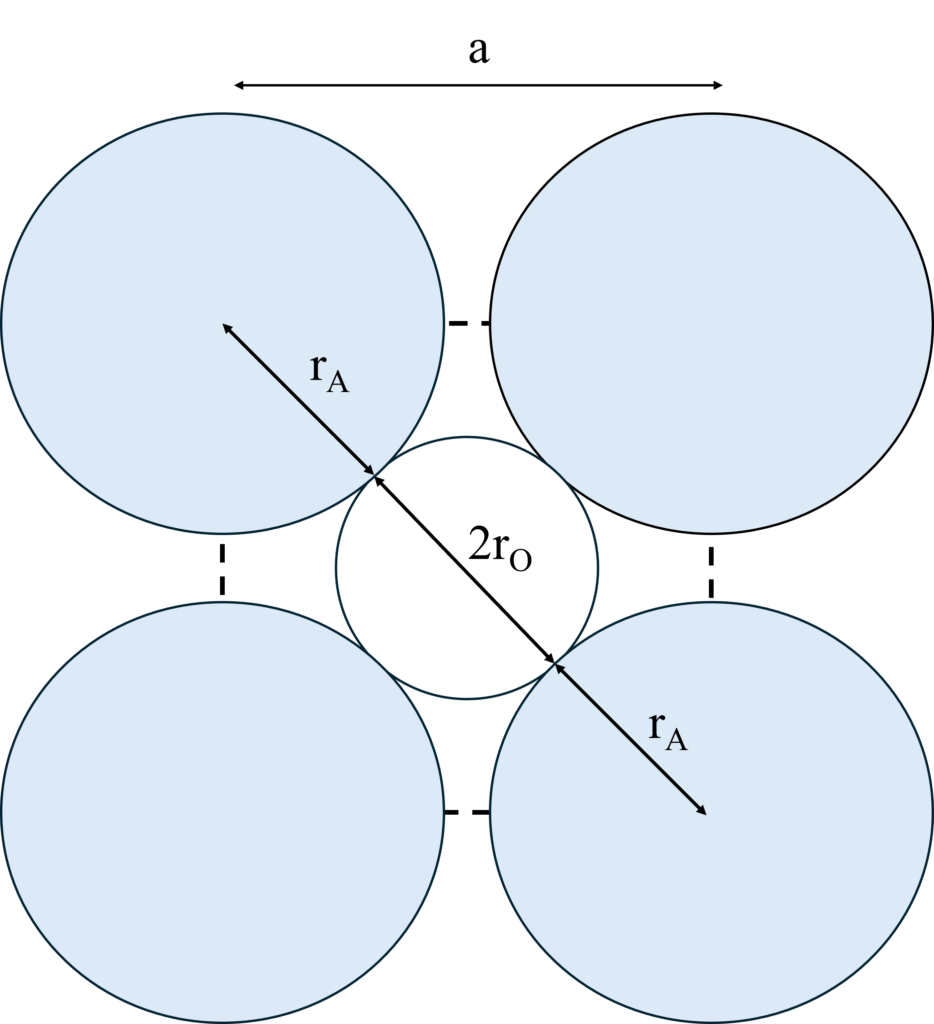
(b) AとOが接している時、下図のようになる。したがって、下図より、
$\sqrt 2 \,a = 2\left( {{r_A} + {r_O}} \right)$
が成り立つ。
これに(a)の結果を代入すると、
$\sqrt 2 \, \times 2\left( {{r_B} + {r_O}} \right) = 2\left( {{r_A} + {r_O}} \right)$
$\therefore \,\,\sqrt 2 \,({r_A} + {r_O}) = {r_B} + {r_O}$
となる。
解説
①~③の問題まで、一気に解説します!
配位数について、こちらの図を見ると分かりやすいです。
『シュライバー・アトキンス無機化学(上) (第6版)』 p100より
図から分かるように、Bは6個の原子と近接しており、Aは12個の原子と近接しています。
また、AイオンとOイオンから構成される面心立方格子の中心をBが占有すると、ペロブスカイト構造になります。
これは、問題文の図からもわかりやすいですね!
このペロブスカイト型構造ですが、AイオンとOイオンから構成される層とBイオンとOイオンから構成される層の2層があります。
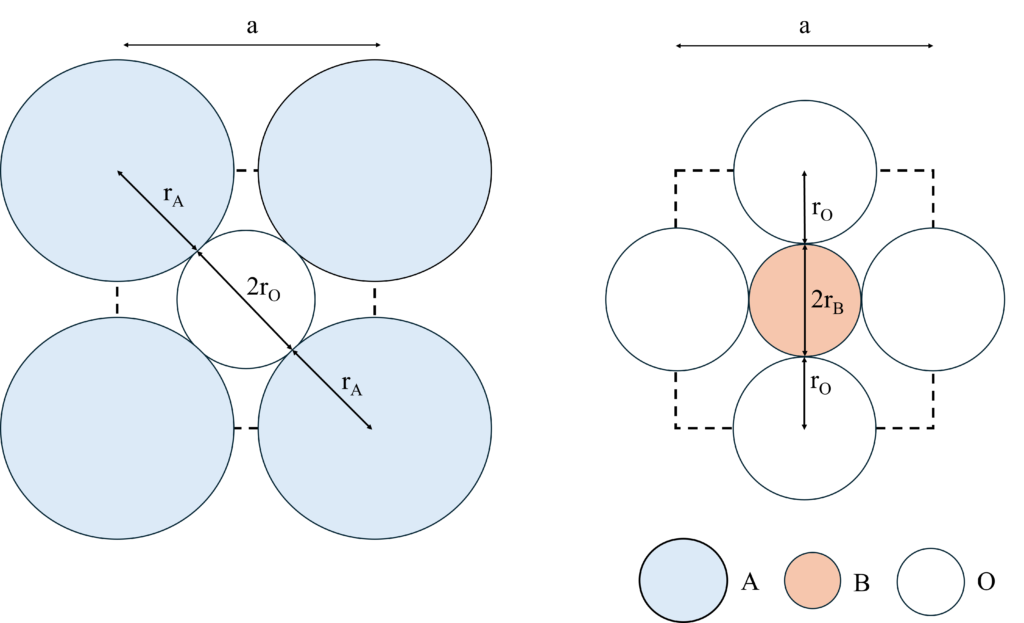
(a)は右図より、
$a = 2\left( {{r_B} + {r_O}} \right)$
です。
図さえ書くことが出来れば(a)と(b)ともに解くことが出来ると思います!
Ⅱ-2 (2)
①
キ 2H+
ク H2
解説
還元反応による水素発生の半反応式なので、これはおそらく高校化学の知識で書けるはずです!
②
ケ 2H2O
コ O2
サ 4H+
解説
液性の指定がないため、OH–を使わないことに注意しましょう。
H2Oから酸素が発生する半反応式を書きます。
③
下線部オと下線部カの半反応式の標準電極電位をそれぞれ${E_1}$と${E_2}$とすると、
$4{H^ + } + 4{e^ – } \to 2{H_2}\,\,{E_1}$
$2{H_2}O \to {O_2} + 4{H^ + } + 4{e^ – }\,\,{E_2}$
電池電位 ${E_{cell}} = {E_1} – {E_2} = – {E_2} = – 1.23$
$\therefore \,\,{E_2} = 1.23\,V$
となる。ここで、水の分解の全反応式の標準反応ギブズエネルギーをΔrG’とすると、
${\Delta _r}G’= – \nu F{E_{cell}}= – 4 \times 9.65 \times {10^4} \times ( – 1.23)$
≒$475\,kJ\,mo{l^{ – 1}}$
であり、各分子の標準生成ギブズエネルギーを用いて
${\Delta _r}G’ = {\Delta _f}G({O_2}) + 2{\Delta _f}G({H_2}) – 2{\Delta _f}G({H_2}O) = – 2{\Delta _f}G({H_2}O)$
と書ける。
ここで、下線部カの標準反応ギブズエネルギーをΔrGとして標準生成ギブズエネルギーを用いて記述すると、
${\Delta _r}G = 4{\Delta _f}G({O_2}) + {\Delta _f}G(4{H^ + }) – 2{\Delta _f}G({H_2}O) = – 2{\Delta _f}G({H_2}O)$
であるから、以上より、
${\Delta _r}G$=${\Delta _r}G’$≒$475\,kJ\,mo{l^{ – 1}}$
となる。
解説
・電池電位と電極電位
・反応ギブズエネルギーと生成ギブズエネルギー
を使い分けるようにしましょう!
また、${\Delta _r}G’= – \nu F{E_{cell}}$の式の$E$は電池電位であることに注意してください!
Ⅱ-2 (3)
①
シ 3
ス 1
解説
まず、Mnの電子配置は[Ar]3d54s2であり、Mn3+の電子配置は[Ar]3d4となります。
すなわち、d電子を4つ保有していると言えます。
これを各軌道に分配していきますが、ここで重要となるのはMnについて八面体錯体であると考えることが出来る点です!
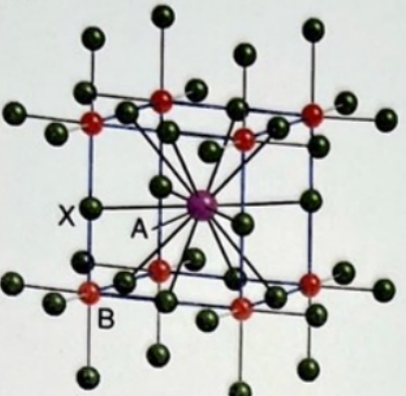
まず、八面体錯体はこちらの図のように、金属を中心として各座標軸上に2つの配位子が配置されています。
(1)の図を見ると、Mn((1)図のB)を中心としてOがこのように配置されていますよね。
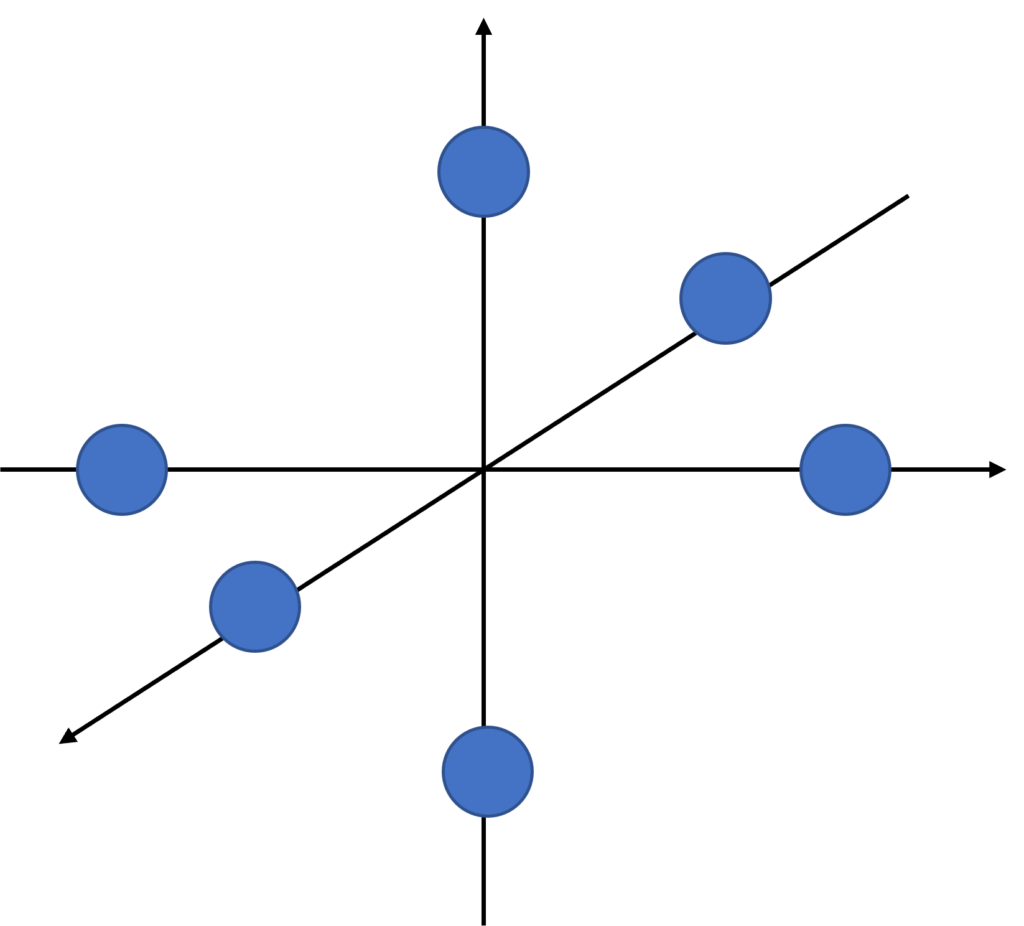
したがって、Mnについて八面体錯体と考えることが出来ます。
八面体錯体のd軌道の分裂については、こちらの記事で解説しました。

結論をまとめると、d軌道は低エネルギーのd軌道3本が縮合したt2g軌道と高エネルギーのd軌道2本が縮合したeg軌道に分裂します。
4つのd電子が1つずつ軌道に入るので、t2g軌道に3個、eg軌道に1個の電子が占有します。
②
セ 超交換
タ 二重交換
解説
まず、超交換相互作用とは、
磁性カチオンの間に位置するアニオンを介在して働く磁気相互作用
のことを言います。
こちらの図のように、一方のカチオンの上向きの全スピンは酸素のp軌道の下向きスピンと相互作用し、他方のカチオンでも同様に相互作用します。
その結果、このようにカチオン同士は反並行に磁気モーメントが配列するので、反強磁性体となります。
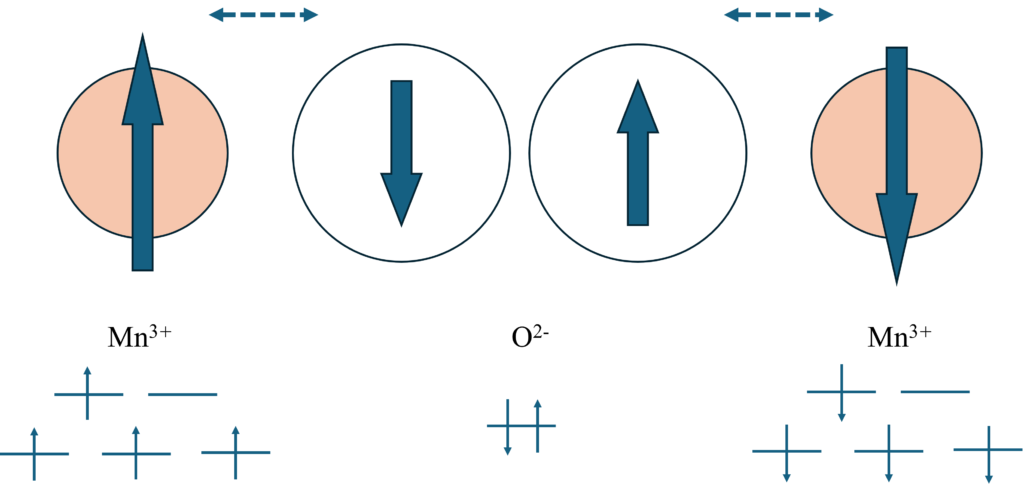
一方で、二重交換相互作用も超交換相互作用と類似していますが、カチオンが異価数であることがポイントです。
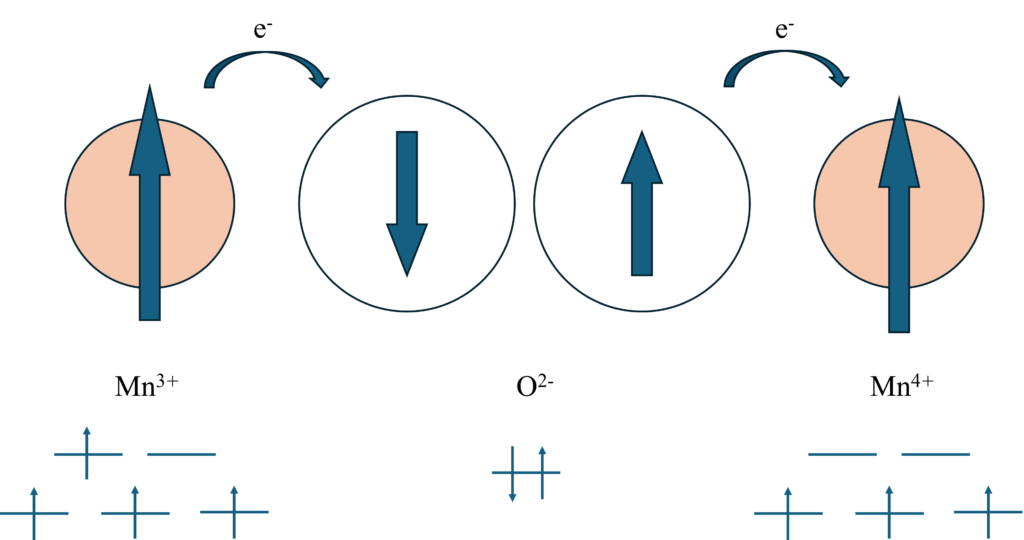
この相互作用機構では、下図のようにMn3+イオンは隣接するO2-イオンに1電子を渡そうとします。
しかし、p軌道は閉殻であるため、これを可能にするためにO2-は同時に1電子をMn4+に渡すことになります。
この電子のホッピングにより、2つのカチオン間のスピンが並行で安定となり、結果として強磁性体を示すことになります。
③
F
解説
eg軌道は酸素方向に伸びているため(エネルギーが高いのはこのためです)、酸素のp軌道と相互作用できます。
したがって、Oの2p軌道とMnのeg軌道の組み合わせであるFが正しいです。
④
チ Fe3+
ツ Fe3+
テ Ni2+
2価の第一系列遷移金属イオンM2+とFe3+を1:2で含む、『MFe2O4』がスピネル型フェライトの1つとしてよく知られています。
このスピネル型フェライトの単位格子には、32個のO2-、8個のM2+、16個のFe3+が存在しています。
また、八面体位置にM2+とFe3+が、四面体位置にはFe3+のみ配置しています!
⑤
全スピン量子数Sは不対電子の数をNとすると、
$S = \frac{1}{2}N$
と書くことが出来るので、それぞれの不対電子の数を考えればよいです。
ここで、各元素の不対電子の数は、
Fe3+…[Ar]3d5より、5個
Ni2+…[Ar]3d8より、2個
となります。
ただし、注意が必要なのがスピンの向きです。
四面体位置のカチオンFe3+と八面体位置のカチオンFe3+とNi2+はスピンが反対向きであり、八面体位置のカチオン同士はスピンが並行です。
したがって、
S=-5/2(四面体位置のFe3+)+5/2(八面体位置のFe3+)+2/2(八面体位置のNi2+)=1
よって、S=1となります。
⑥
フェリ
解説
(今回の四面体位置と八面体位置のように)磁気モーメントが互いに逆向きでも、磁気モーメントの大きさが異なることで総和が0にならずに磁化が発生するようなものを、『フェリ磁性』と呼びます。
最後に
いかがでしたか?
今回は、2024年度東京科学大院試の応用化学系の無機化学の問題について解説してきました。
今後も過去問の解説をどんどんしていきますので、ぜひ参考にしてみてくださいね!












コメント