皆さんは、
東工大院試に向けて過去問を解いているけど、難しい!
過去問の解答が欲しい!
と思っていませんか?
この記事では、2024年入学東工大の物質理工学院応用化学系の無機化学の問題解答について、解説していきます!
問題(Ⅰ-2)はこちら(東工大ホームページ)からダウンロードできます。
ぜひ、問題を解いてから読んでみてください!
こちらの解答は正式なものではなく、筆者が出した解答ですのでその点には十分注意してお読みください!


Ⅰ-2(1)
①
ア 4s
イ 4p
ウ dx2-y2 dz2
エ 非結合性
オ dxy dyz dzx
解説
配位子場理論の問題は頻出です!
あまりちゃんと理解できていない方は、ここでしっかり覚えておきましょう!
八面体を形成する中心金属原子の軌道は、対称性によって4つの組に分けることができます。
s軌道…a1g
px py pz 軌道…t1u
dx2-y2 dz2 軌道…eg
dxy dyz dzx 軌道…t2g
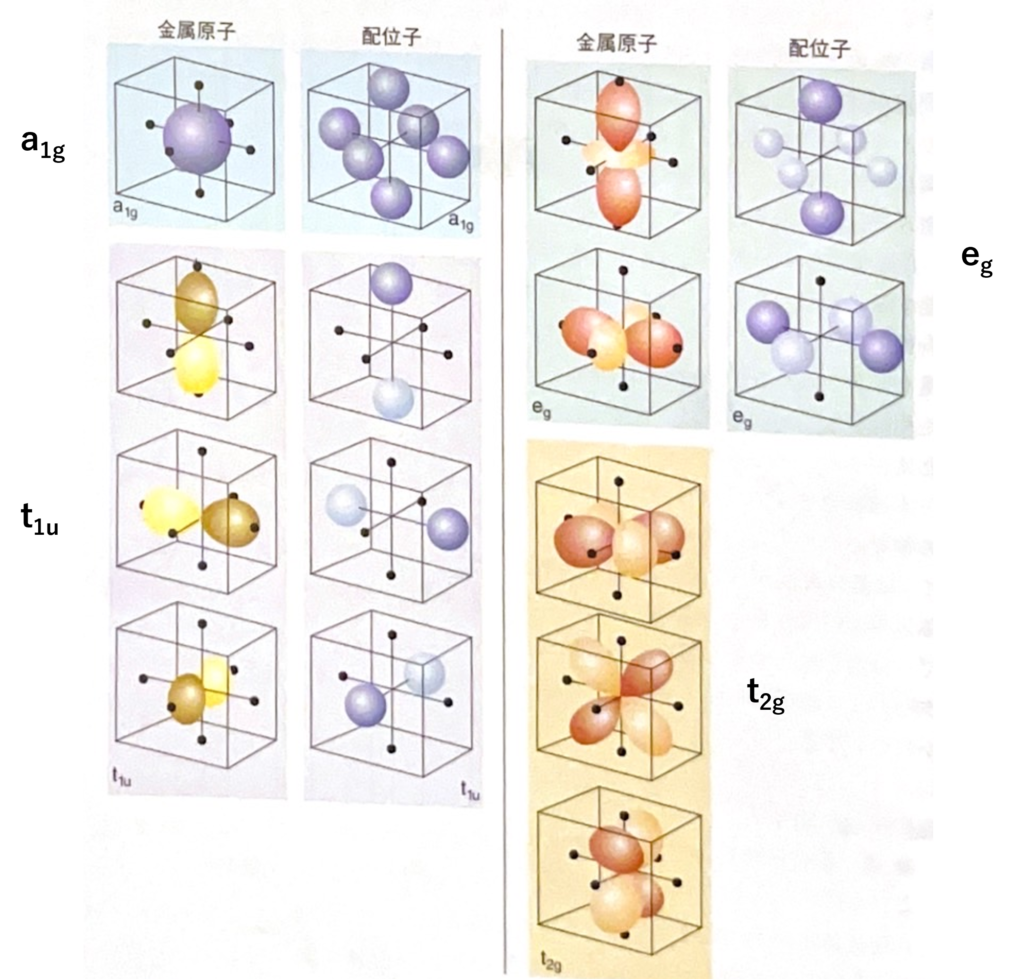
(『シュライバー・アトキンス無機化学(下)第6版』 p618より引用)
これらの組み合わせの対応はしっかり記憶しておきましょう!
これを念頭に、今回の問題と対応させていきます。
まず、3d金属の場合、配位子との相互作用に関与してくる原子軌道は比較的外側の電子殻にある3d軌道、4s軌道、4p軌道です(それより内側の軌道はエネルギーが低いため、相互作用が幾分小さいため)。
したがって、先ほどの知識も頭に入れて、
a1gと相互作用が強い原子軌道は、4s軌道(ア)
t1uと相互作用が強い原子軌道は、4p軌道(イ)
となります。
また、egとの対称性が合致するのは、先ほど記載した通り、dx2-y2 と dz2 軌道(ウ)です。
続いて、σ結合性とπ結合性について、
結合軸に沿っているような軌道である、a1g、t1u、egはσ結合性を持ちます。
一方で、t2gはσ結合性がありません。
例えば、dx2-y2(eg)とdxy(t2g)を考えてみると、
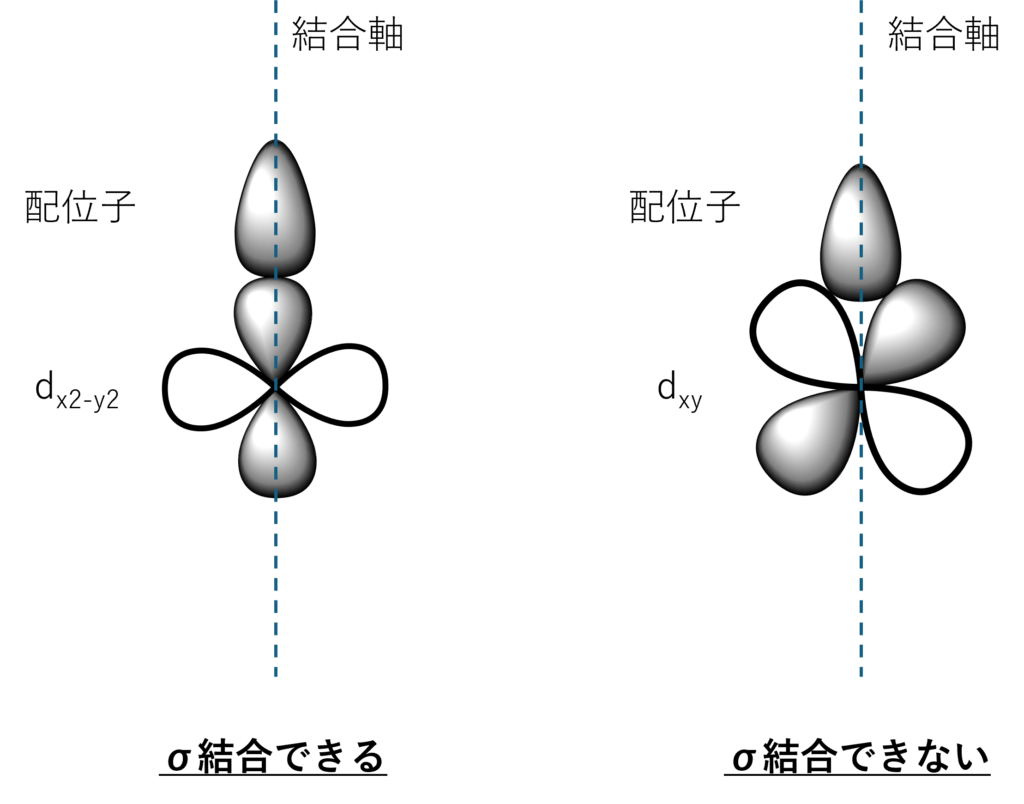
上図のように、配位子が結合軸から近づいて来たときに、dx2-y2は軌道が合致して結合できますが、dxyでは軌道が合致せず、結合できません。
したがって、今回の問題に適応すると、t2gは非結合性(エ)となります。
同様に、π結合の場合を考えてみましょう!
先ほどとは逆に、t2gはπ結合性がある一方で、a1g、t1u、egはπ結合性を持ちません。
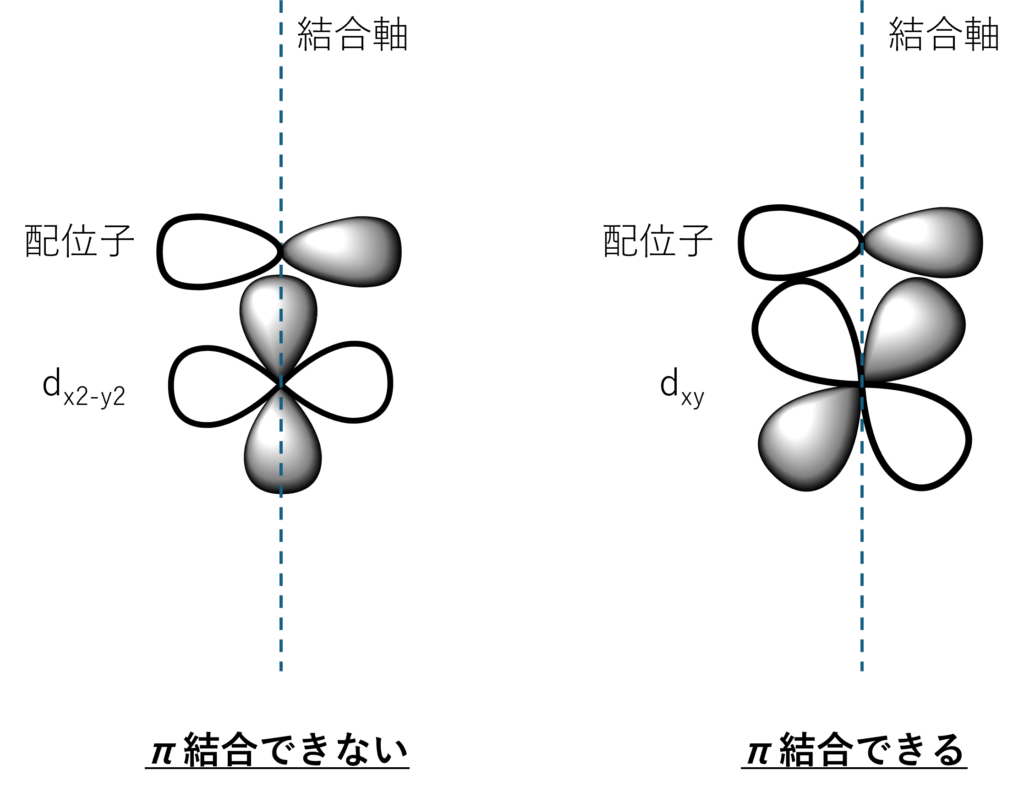
dx2-y2 (eg)は軌道が合致せずに結合ができずに、dxy (t2g)では軌道が合致して結合ができることからもわかりますよね!
以上のことから、COのπ*軌道と相互作用する3d軌道はdxy dyz dzx 軌道(オ)と結論づけることができます。
②
A
解説
まず、八面体錯体の典型的な分子軌道のエネルギー準位の図はこちらのようになります。
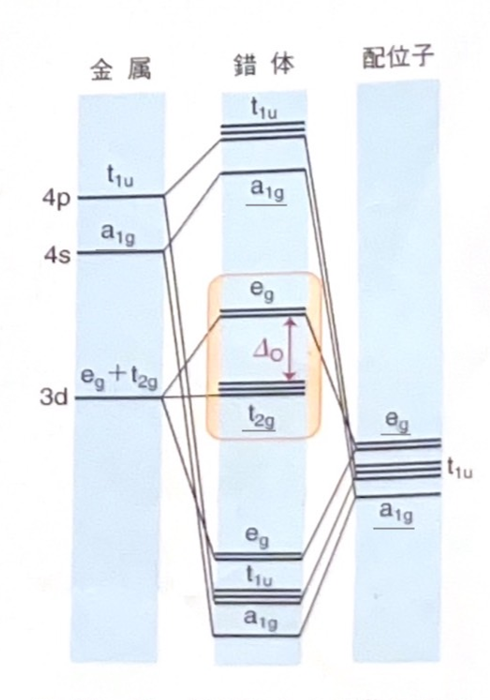
(『シュライバー・アトキンス無機化学(下)第6版』 p619より引用)
配位子との相互作用がより強いということは、結合性軌道(eg)がより大きく安定化し、そのエネルギー分反結合性軌道(eg*)が大きく不安定化するということです。
つまり、eg*軌道のエネルギーが高く(ⅰ)なり、その結果としてHOMO-LUMOギャップは大きく(ⅱ)なります。
よって、解答はAと結論づけることができます。
➂
Cr
解説
『錯体の電子数の数え方』については違うサイトにはなるのですが、実はこちらの記事で解説しています。

簡単にまとめると、配位子には共有結合性を持つX型配位子と配位結合性を持つL型配位子の2種類があり、COは後者のL型配位子に該当します。
一般に、錯体の電子数について以下が成り立ちます。
一般式を[MXaLb]c+、金属の族数をNの時、
総電子数=N+a+2b-c(=N+2a+2b-(a+c))
よって、今回の問題の場合は総電子数が18であるので、
18=N+0+2×6-0
∴N=6
よって、6族の3d金属はCrであることから、解答はCrと結論づけることができます。
錯体の電子数の数え方に不安がある方は、ぜひ先ほどご紹介した記事も参考にしてみてくださいね!
④
d軌道よりもエネルギー準位の高いCOの空のπ*軌道とd軌道が相互作用して結合性軌道が生じる。この軌道のエネルギーはもとのd軌道のエネルギーより低い。したがって、HOMO-LUMOギャップは大きくなる。
解説
配位子との相互作用とHOMO-LUMOギャップの大きさには関係性があり、
相互作用する配位子の種類(π供与体配位子とπ受容体配位子)により、HOMO-LUMOギャップの大きさが変化します。
π供与体配位子…結合前からπ軌道が占有されている配位子(Br– ,Cl– , OH–,H2Oなど)
π受容体配位子…電子を受け入れられる空のπ軌道を持つ配位子(CO, N2など)
・π供与体配位子の場合
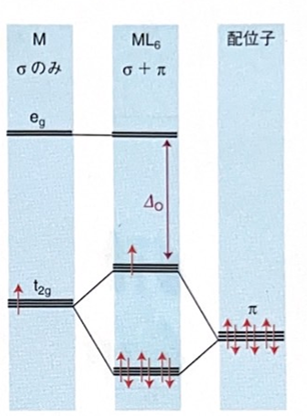
(『シュライバー・アトキンス無機化学(下)第6版』 p621より引用)
配位子のπ軌道は通常金属のd軌道のエネルギーより低いです。
π軌道とd軌道が相互作用することによって結合性軌道と反結合性軌道が生じ、π軌道の電子は結合性軌道に、d軌道の電子は反結合性軌道に入ります。
したがって、HOMO-LUMOギャップ(図でいうと⊿o)は小さくなります。
・π受容体配位子の場合
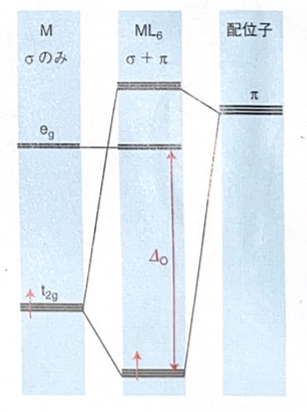
(『シュライバー・アトキンス無機化学(下)第6版』 p621より引用)
一方で、こちらの場合は配位子のπ軌道は通常金属のd軌道のエネルギーより高いです。
同様に、π軌道とd軌道が相互作用することによって結合性軌道と反結合性軌道が生じ、d軌道の電子が結合性軌道に入ります。
したがって、HOMO-LUMOギャップは大きくなります。
今回の問題では、CO(π受容体配位子)との相互作用についてなので解答のように記述することができます!
⑤
金属カルボニルでは、金属原子MからCO配位子へと電子が供与されるπ逆供与結合の寄与が大きい。つまり、この供与が小さいとM-COの結合は弱くなる。紫外線照射によって、COのπ*軌道と相互作用できるd軌道の電子が昇位するため、この電子密度は低下する。よって、M-COの結合は弱くなるため、CO配位子の脱離が促進される。
解説
正直、これに関してはあまり自信がありません。…が、おそらく解答のようになるんじゃないかな?と考えています。
COが金属に配位するとき、CO→Mへ電子を供与するσ結合とM→COへ電子を供与するπ逆供与結合の2つからなりますが、後者の方が寄与が大きいです。
なぜなら、COは求核性が低く、電子供与体としては非常に弱いからです。
つまり、M-COの結合の強さは金属からのd電子供与(π相互作用なのでt2g軌道の電子供与)で決まるということができます。
紫外線が照射されるとt2g軌道にある電子が昇位するので、逆供与できるt2g軌道の電子密度が低下し、M-COの結合の強さは低下します。
したがって、COは紫外線照射によって脱離しやすくなると考えました。
⑥
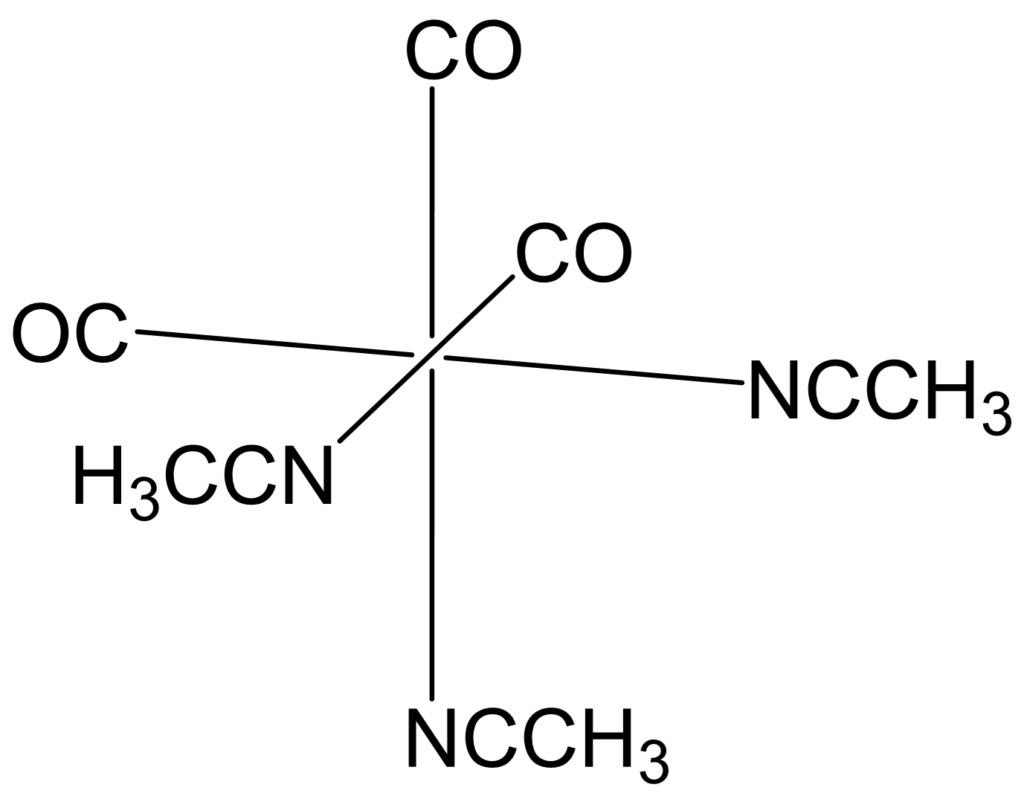
解説
[MA3B3]型の八面体錯体では、mer異性体とfac異性体という2つの異性体が存在します。
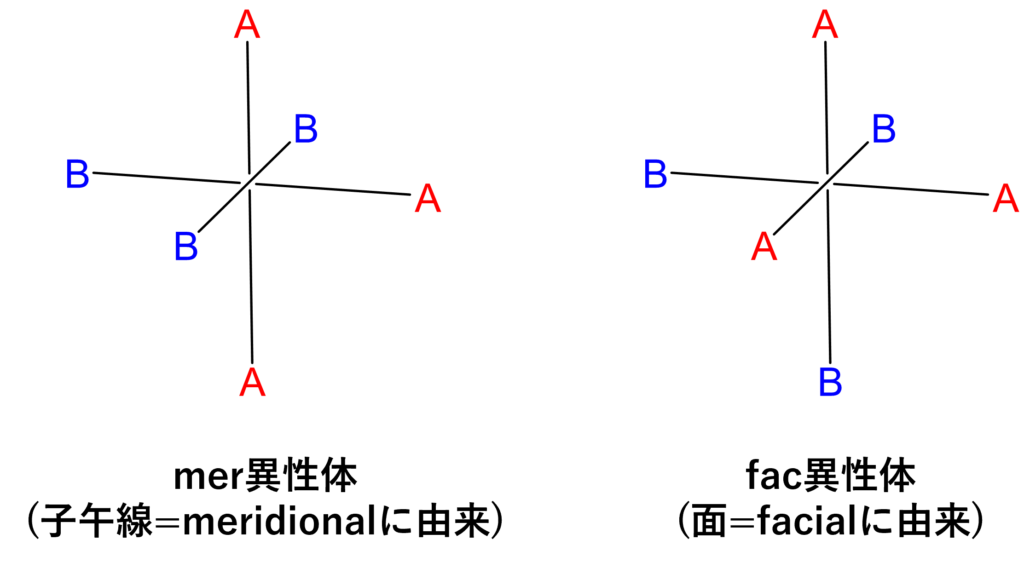
配位子の置換に関する問題で、『トランス効果』を題材にした問題はよく出てきますが、トランス効果は一般に平面四角形錯体での話なので、今回の八面体錯体で適用できません。
トランス効果…ある配位子がそのトランス位にある他の配位子を置換させやすくする現象
八面体錯体(特に金属カルボニル)の配位子置換で知識として知っておきたいのが『シス効果』です。
シス効果とは、トランス効果とは逆である配位子がそのシス位にある他の配位子(特にCO配位子)を置換されやすくする現象のことです。
頻出ではないと思いますが、ぜひ知らない方はこの機会に覚えておきましょう!
今回の問題に適用すると、シス位のCOが置換されやすくなるので、
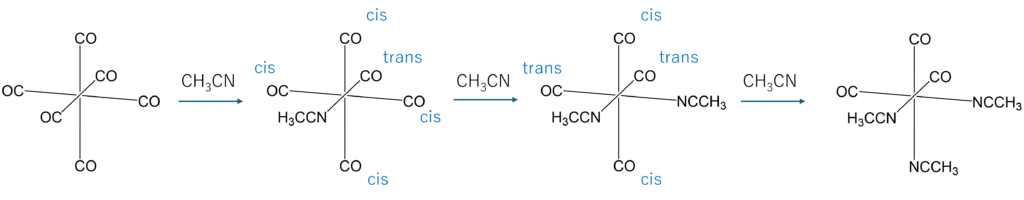
というように、シス位のCOが置換されるので最終的にfac異性体の[M(CO)3(CH3CN)3]が得られると結論づけることができます。
Ⅰ-2(2)
①
(ⅲ)
解説
ホウ素化合物は院試で頻出です!
その理由として、
・BH3は二量体を形成するため
・BX3(X=F, Cl, Br)の酸性度は電気陰性度から予想されるものと逆になるため
が挙げられます。
しかし、しっかりとホウ素化合物について勉強していればこの①~➂は得点源になります。
覚えていない方はここで一気におさえておきましょう!
まず、問1については当然構造を覚えているかどうかがカギです。
(ⅱ)と(ⅲ)のどちらか一見迷いますが、ジボランは全ての水素が同一平面上にないことに注意して、(ⅲ)を選択しましょう!
②
sp2
解説
必ず得点しておきたい問題です。
ホウ素の電子配置は[He]2s22p1であり、2s軌道の電子が1つp軌道に昇位してs,p,pの3つの電子から混成軌道ができるので、三フッ化ホウ素の混成軌道はsp2と結論づけることができます。
平面三角形構造をしていることからも、sp2混成軌道と予想することができますよね!
➂
三ハロゲン化ホウ素のハロゲン原子はホウ素の空の2p軌道とπ結合を形成するが、このπ結合が強いと空の2p軌道の電子求引性は弱まり、ルイス酸性度は低下する。FとBrを比較すると、Fは2p軌道でBrは3p軌道で重なるため前者の方が重なりやすく、π結合が強い。したがって、三臭化ホウ素の方がより強いルイス酸である。
解説
①の解説でも述べましたが、この酸性度を考える問題も頻出です!
電気陰性度のみで考えると、Fの電気陰性度が最も大きいのでBがより電子欠乏となって強い酸として振る舞うと結論づけたくなります。
しかし、実際は問題文にもあるようにBF3の方が弱いです。
まず、ホウ素は空の2p軌道を有しており、塩基と反応する際はこのp軌道に電子が流入します。
つまり、空の2p軌道の電子求引性が高いほど、強い酸性度を示すということができます!
また、BX3(X=F, Cl, Br)について、ハロゲンのp軌道とホウ素の空のp軌道はp-pπ結合をしており、塩基と反応する際はこのπ結合が切断される必要があります。
つまり、π結合が強い=空のp軌道は塩基と反応しにくい=ルイス酸性が弱いとなります。
ここで、F, Cl, Brの電子配置を比較すると、π結合を形成するのは2p, 3p, 4pであり、明らかにFの2p軌道がホウ素の空の2p軌道と重なりが強く、π結合も強いです。
したがって、酸性度はBF3 < BCl3 < BBr3の順となり、解答のように結論づけることができます!
最後に
いかがでしたか?
今回は、2023年度東工大院試の応用化学系の無機化学の問題について解説してきました。
今後も過去問の解説をどんどんしていきますので、ぜひ参考にしてみてくださいね!












コメント
コメント一覧 (6件)
こんばんは!
今回もタメになる記事をありがとうございます。
無機化学特に苦手な科目だったので、参考にしてがんばります!
かめ様
コメントいただき、ありがとうございます。
無機化学は要点をおさえていけば点を取れると思うので、ぜひ過去問演習を頑張ってください!
今後も、当ブログをよろしくお願いします。
配位子場理論苦手だったので参考にして勉強させて頂きます
これからも為になるコンテンツ期待しています
azt様
コメントいただき、ありがとうございます。
配位子場理論、難しいですよね。結晶場理論とも近いところがあるので、ぜひこちらの記事も合わせて参考に勉強してみてください!
https://wind-perc.com/crystal-field-theory/
今後とも当ブログをよろしくお願いします。
無機化学の解説をリクエストさせていただいた抹茶です。
無機化学の解説ありがとうございました!分かりやすかったです!
違うサイトの記事も勉強になりました
抹茶様
コメント及び先日はリクエストしていただき、ありがとうございました。
そう言っていただけると、とても励みになります!
院試勉強、とても大変だと思いますが頑張ってください!
今後とも当ブログをよろしくお願いします。