皆さんは、
東京科学大院試に向けて過去問を解いているけど、難しい!
過去問の解答が欲しい!
と思っていませんか?
この記事では、2024年入学東京科学大の物質理工学院応用化学系の有機化学の問題解答について、解説していきます!
問題(Ⅰ-1)はこちら(ホームページ)からダウンロードできます。
ぜひ、問題を解いてから読んでみてください!
こちらの解答は正式なものではなく、筆者が出した解答ですのでその点には十分注意してお読みください!

Ⅰ-1(1)
①
1個
解説
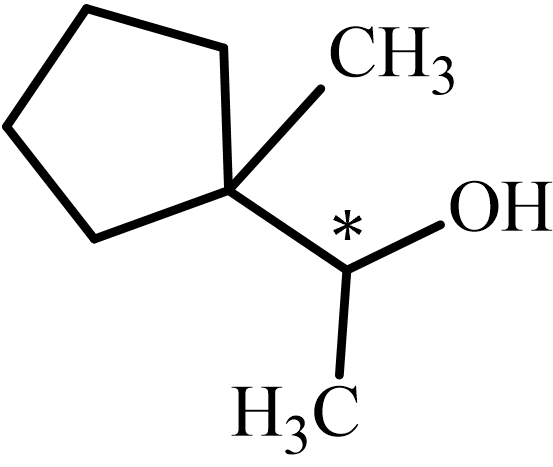
キラル中心の数を数える問題です。
実は、昨年度もキラルの数を解答する問題が出題されています。
環状構造のキラルは一見悩むかもしれません。
しかし、今回の化合物は1位のみに置換基がついているシクロペンタンです。
この場合、環上に不斉炭素は存在しません。
なので、下記のように*がついている炭素のみが不斉炭素原子なので、その数は1となります。
②
B

C

解説
カルボカチオン転移を考慮した問題です。
反応機構は下図のようになります。
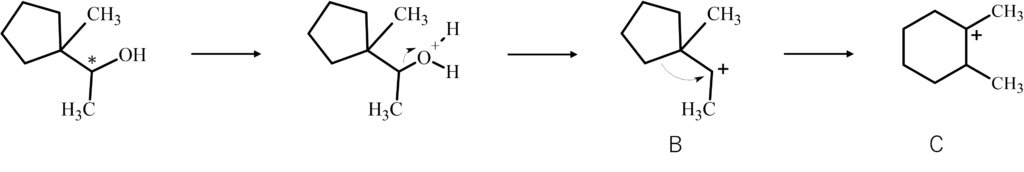
まず、プロトンが-OHに付加してH2Oが脱離すると化合物Bのような第二級カルボカチオン中間体となります。
ここで、カルボカチオンの安定性は、
第三級>第二級>第一級
の順番です。
なので、より安定な中間体になるために転移反応が起こります。
CはDの前駆体であり、Dは1,2-ジメチルシクロヘキセンであることから、どのような転移反応が起こるのか読み取りましょう!
そうすると、上のように転移反応が起こることで、化合物Cのような第三級カルボカチオン中間体が生成します。
➂
解説
立体を考慮した、水素付加の問題です。
二つの置換基が二重結合に付加する場合、
シン付加とアンチ付加があります。
シン付加…二つの置換基が二重結合の同じ側から付加する
アンチ付加…二つの置換基が二重結合の反対側に付加する
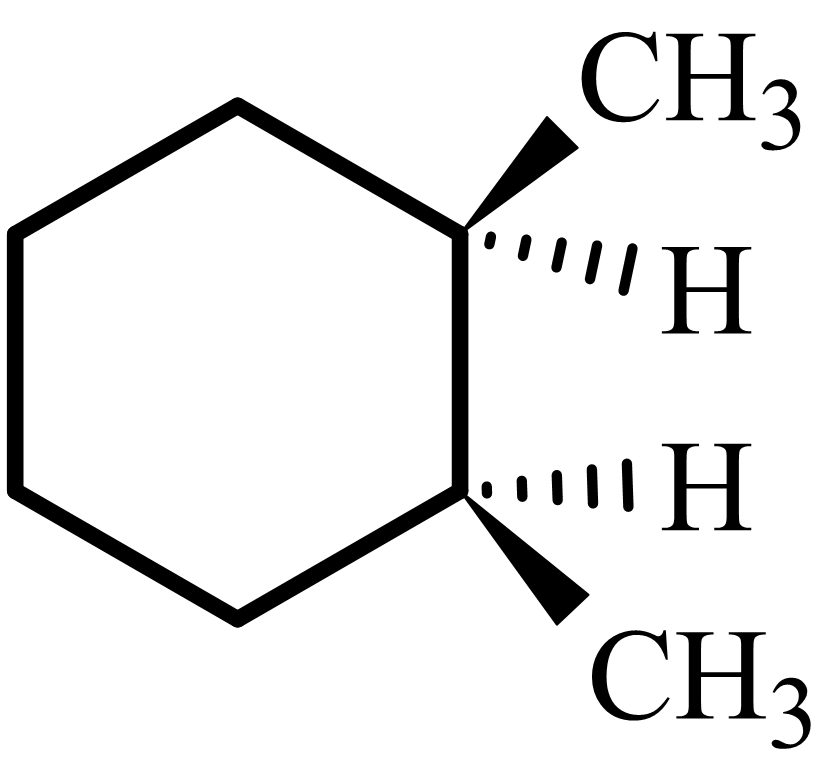
水素付加はシン付加です。
したがって、二つの水素原子は二重結合の同じ面に付加するので、解答のような化合物になります。
④
解説
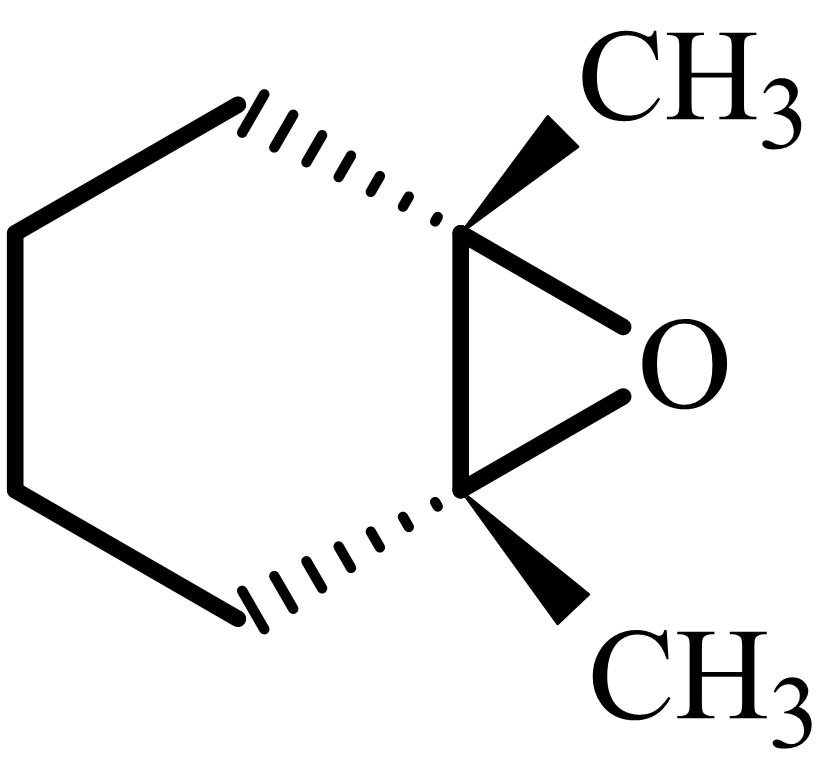
同様に立体を考慮した、エポキシ化の問題です。
mCPBAは過酸の1種であり、エポキシ化に広く用いられます。
また、アルケンは過酸によってエポキシドに酸化されることを思い出しましょう!
過酸付加は水素付加と同様にシン付加なので、化合物Fは解答のようになります。
⑤
解説
オゾン分解の問題です。
これらの試薬を反応させるアルケンに反応されるのは、いわゆる『オゾン分解』となります!
オゾン分解をすることによって二重結合が分解して、カルボニルが生成します。
よって、化合物Gは解答のようになります。
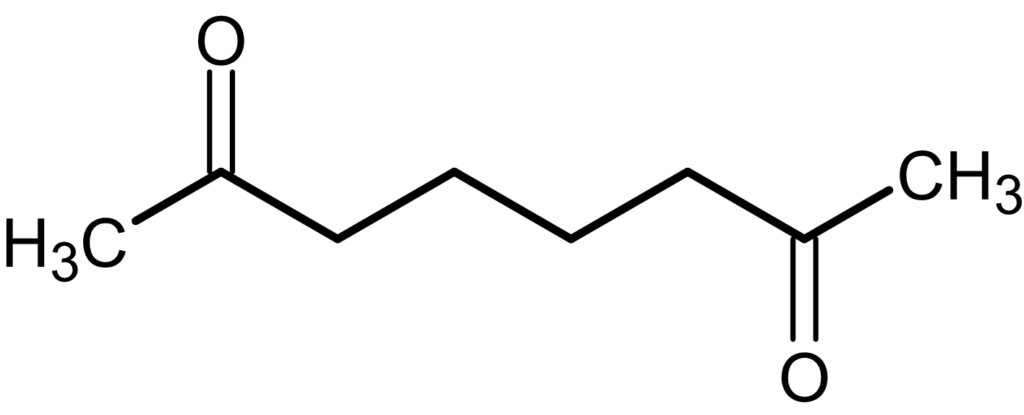
⑥
解説
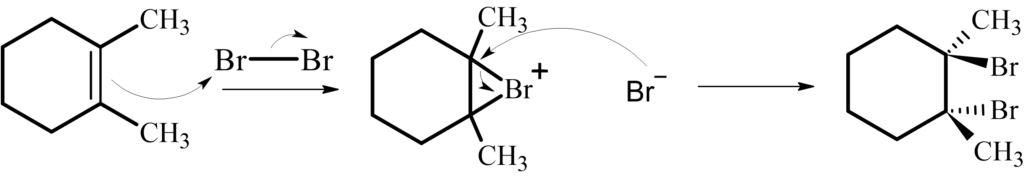
臭素付加の問題です。
ここで、臭素付加はアンチ付加であることに注意しましょう。
反応機構は解答のようになり、最終的に得られる化合物の立体異性体は臭素が互いに反対になることに注意してください!
⑦
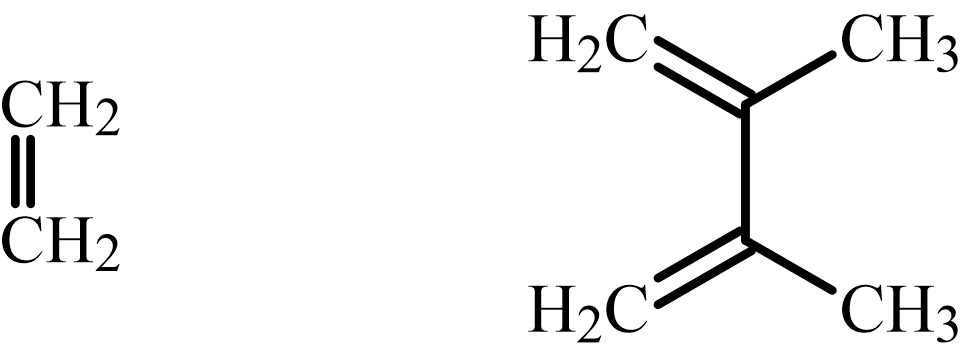
付加環化反応によって二重結合を持つ環ができるということから、Diels-Alder反応を連想しましょう!
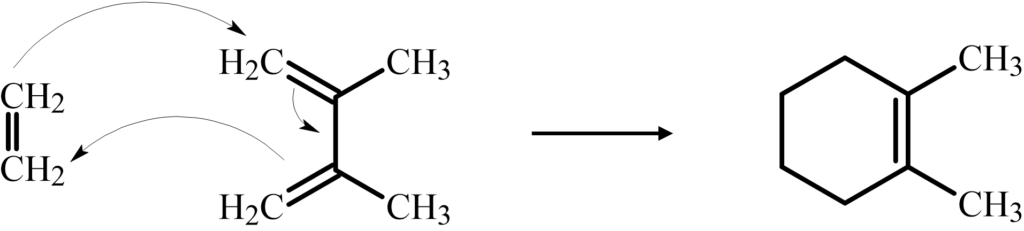
上記のように、この2つの試薬が反応することによって1,2-ジメチルシクロヘキセンが得られます。
よって、試薬Iと試薬Jはエチレンと2,3-ジメチル-1,4-ブタジエンとなります。
Ⅰ-1(2)
①
H3PO2
解説
覚えているか否かで得点の有無が決まる問題です。
アレーンジアゾニウム塩に対して次亜リン酸(H3PO2)で処理すると、ジアゾニウム基が水素で置き換わります。
ベンゼン環の特定の位に置換基をつける際に役立つ反応なので、ぜひ覚えておきましょう!
②
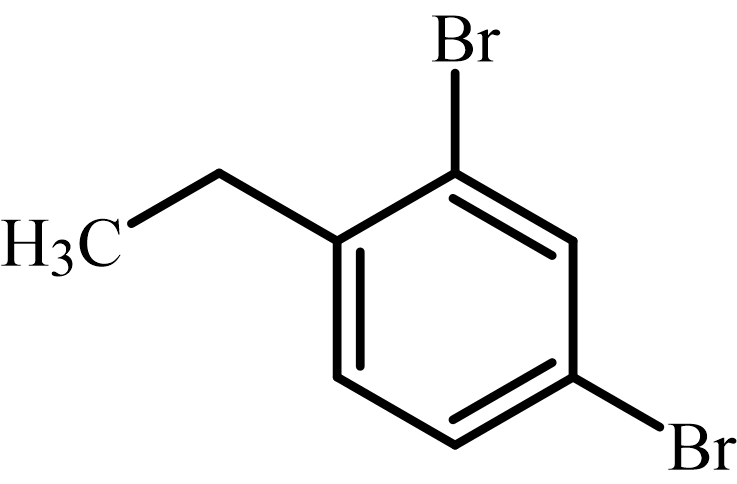
解説
配向性と立体障害を考える問題です。
Brが置換される可能性があるのは、エチル基のo,p配向性より、2,4,6位のうち2つになります。
どこが置換されるのか悩むところですが、ここで考えるべきは立体障害です!
仮に2位と4位についた場合には非常に込み合うことになるため、この2つが置換される可能性は非常に低いと予想できます。
したがって、o位とp位の1つずつが臭素で置換された解答のような化合物になると考えることが出来ます。
➂
化合物N:6、化合物Q:8
解説
13CNMRの問題です。
それぞれの化合物について、異なるCが何個あるのか数え上げればよいです。
そこで重要となるのが対称性です!
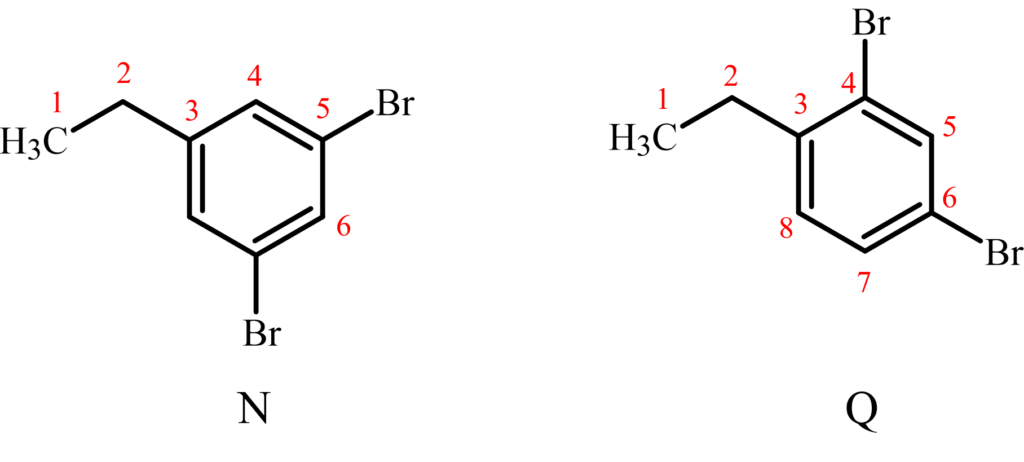
化合物Nは対称性を有しており、上図のように6個の異なる炭素があると言えます。
一方で、化合物Qは対称性を有していないので、全ての炭素が異なるということが出来ます。
以上より、化合物Nは6本のピーク、化合物Qは8本のピークが生じると考えられます。
④
Fridel-Crafts反応はメタ配向基を持つ場合、環が非常に不活性になるため反応が起こらない。アミノ基の孤立電子対は図のように触媒のAlCl3と反応し、メタ配向基となる。よって、反応が進行しなかったと考えられる。
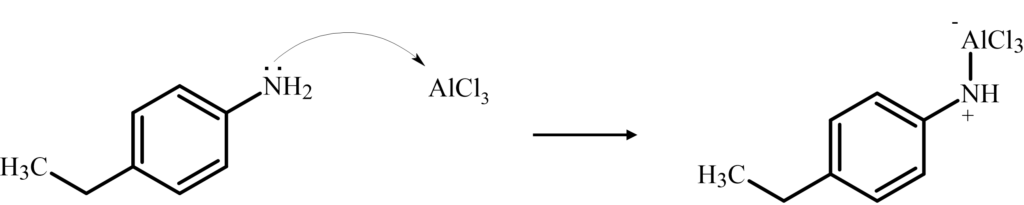
解説
Fridel-Crafts反応と配向性に関する問題です。
Fridel-Crafts反応は、遅い芳香族求電子置換反応なのでベンゼン環が不活性化されていると起こりません。
なので、メタ配向基を持つ場合はFridel-Crafts反応が起こらないという点が重要です!
よって、ニトロベンゼンやベンゼンスルホン酸などはFridel-Crafts反応が起こらないと言えます。
また、Frdel-Crafts反応はLewis酸触媒としてAlCl3が必要ですが、この触媒はNのような強い塩基の孤立電子対と錯体化します。
したがって、アニリンのような場合はNH2がメタ配向基になるので、Fridel-Crafts反応が起こりません。
ただし、Oは弱い塩基なのでLewis酸触媒と錯体を形成しないことに注意しましょう!
よって、フェノールなどは通常通りFridel-Crafts反応が進行します。
⑤
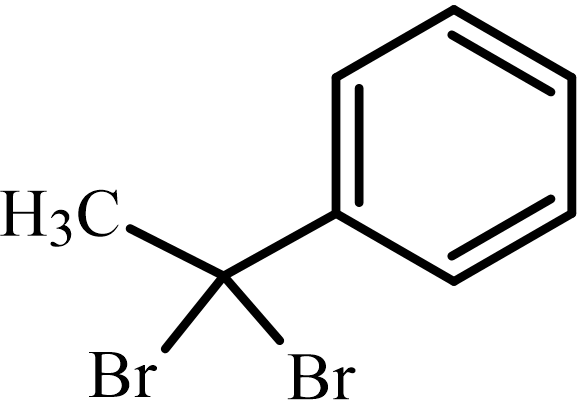
試薬としてNBS(N-ブロモスクシンイミド)を用いているので、Brは臭素ラジカルとして機能します。
反応機構は以下のようになります。
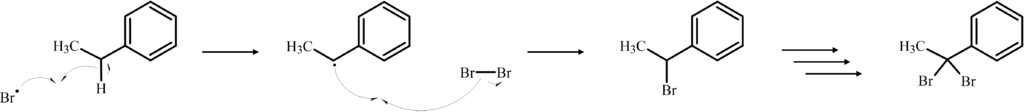
臭素ラジカルは水素を引き抜きますが、このときラジカル中間体が生成します。
ラジカルの相対的安定性は、
ベンジルラジカル≒アリルラジカル>第三級ラジカル>第二級ラジカル>第一級ラジカル
という順番です!
なので、ここで生じるラジカル中間体はより安定なベンジルラジカルになります。
同様に、反応することで解答のような化合物が生成します。
⑥
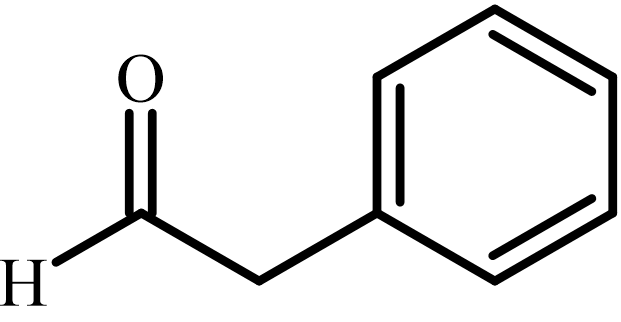
これは、いわゆる『ヒドロホウ素化酸化』です。
反応は以下のようになります。
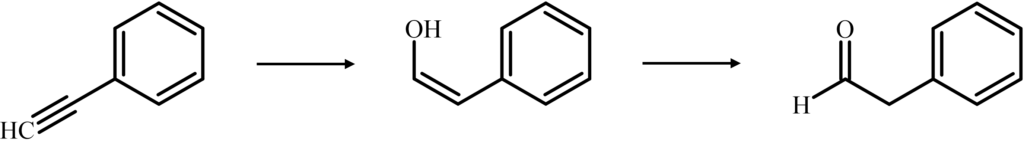
ヒドロホウ素化酸化は『アンチマルコフニコフ則』に従うので、置換基が少ない方に-OHが結合することになります。
また、ここで重要なのはアルキンに反応するということです。
エノールなので、ケト-エノール互変異性によりアルデヒドが生成します。
以上より、化合物Tは解答のようになります。
最後に
いかがでしたか?
今回は、2024年度東京科学大(東工大)院試の応用化学系の有機化学の問題について解説してきました。
今後も過去問の解説をどんどんしていきますので、ぜひ参考にしてみてくださいね!












コメント