皆さんは、
東大院試に向けて過去問を解いているけど、難しい!
過去問の解答が欲しい!
と思っていませんか?
この記事では、2024年度(令和6年度)入学 東大 応用化学科 応用化学専攻の有機化学の問題解答について、解説していきます!
問題(第3問)はこちら(東大ホームページ)からダウンロードできます。
https://www.t.u-tokyo.ac.jp/hubfs/graduate/2024/Past_Entrance_Examinations/C_J_E_2024.pdf
ぜひ、問題を解いてから読んでみてください!
こちらの解答は正式なものではなく、筆者が出した解答ですのでその点には十分注意してお読みください!
Ⅰ.
1.
解答
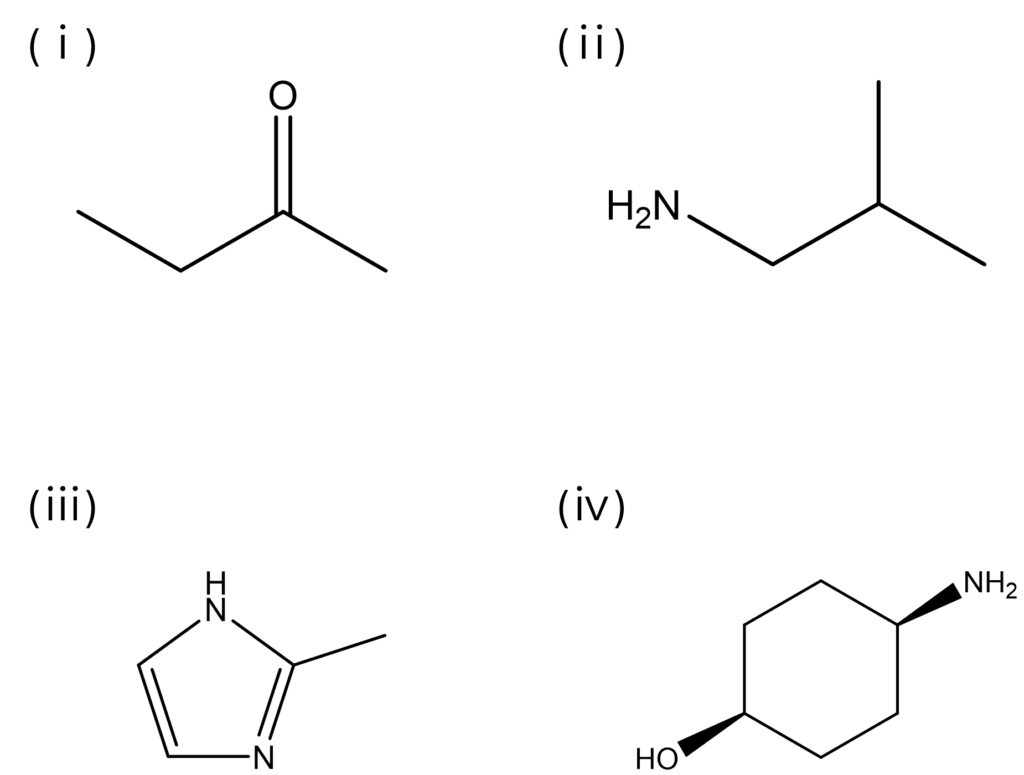
解説
化合物名から構造式を書く問題です。
特筆すべきことは少なく、差がつくとすれば『イミダゾール』の構造式を覚えているかといったところでしょう!
2.
解答

解説
(ⅰ)
Newman投影式は、Fischer投影式を経由してから書くと分かりやすいです。
(1S,2R)-1-クロロ-1,2-ジフェニルプロパンのFischer投影式は下図のようになります。
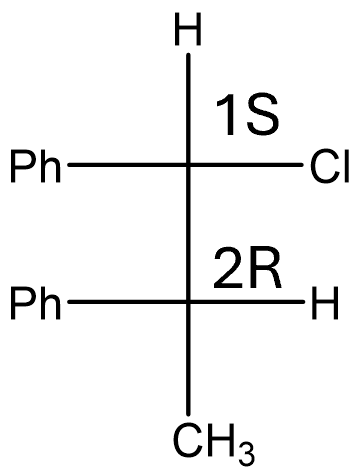
そして、下図のようにFischer投影式を重なり配座のNewman投影式に変換した後、ねじれ配座のNewman投影式に変換すると、解答のようになります!
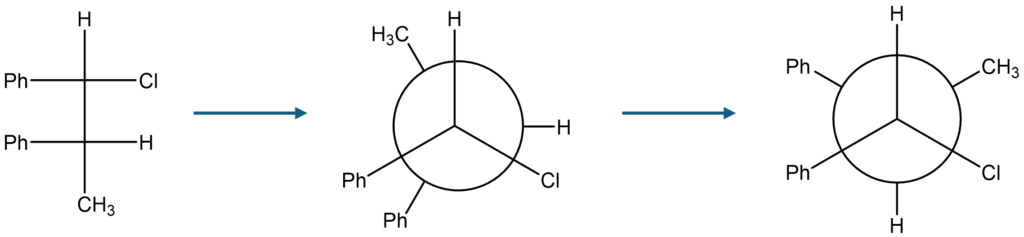
・基を優先順位で適切に配置した時
時計回り…R配置 反時計回り…S配置
(Fiscer投影式では、優先順位が最も低い基が水平方向にある場合は逆になることに注意!)
・Fiscer投影式→Newman投影式
①Fiscer投影式の上方の十字にある基をNewman投影式の手前に持ってくる
②Fiscer投影式の下向きの結合を、Newman投影式の奥の炭素上方に向かう結合にして左右の原子は保持
という2Stepで重なり配座のNewman投影式を書くことができる。
そして、これをねじれ配座になるように回転することでNewman投影式となる。
(ⅱ)
ハロゲン化アルキルの反応なので、置換反応(SN2 or SN1)と脱離反応(E2 or E1)のいずれかかが起こります。
どの反応があるかが主に起こるか最初に考えてみましょう!
まず、第二級ハロゲン化アルキルかつNaOEtという強塩基を用いていることから、E2が優先的に起こって主生成物となります!
次に、立体化学について考えてみます。
通常はより安定なE体(トランス体)が主生成物ですが、今回の化合物のようにE2反応でβ水素が1つの場合は注意が必要となります。
なぜなら、この時は1種類のアルケンのみしか生成しないからです。
この場合は下図のように透視式を描き、アンチ脱離させることで1種類の立体異性体を得ることができます。

今回の場合は、E2反応が起こることで解答のようなE体の脱離生成物を得ることができます!
・置換反応と脱離反応により得られる生成物をまとめると、以下のようになります。

3. (ⅰ)
解答
共役酸
C>B>D>E
芳香族アミンであるEは電子の非局在化により、アルキルアミンよりも塩基性が低い。アルキルアミンのうち、Dでは他方のNの電子求引性誘起効果によって、塩基性が低くなる。また、BとCではBの立体障害が大きいため、Cの方が塩基性が高い。したがって、共役酸のpKaはC>B>D>Eの順になる。
解説
酸・塩基の問題です。
まず、B・C・D・Eを見るとEだけ芳香族アミンで他はアルキルアミンであることが分かります。
アミンの塩基性について
(アルキルアミンの塩基性) > (芳香族アミンの塩基性)
ということは覚えておきたいです!
これは、非局在化によってN上の電子密度が低下するからですね。
したがって、塩基性はB・C・D > Eであることが分かります。
続いて、塩基性の判定で重要となってくるものとして『電子求引性誘起効果』というものがあります。
塩基は電子による求核攻撃のしやすさともいえるので、これが起こると電子密度が低下する=塩基性が低下するので重要です。
B・C・Dのうち、DのみNが2つあって一方のNの電子を他方のNが電子を求引することが想像できます。
したがって、塩基性はB・C > Dであると判断できます。
最後に、重要となるのが立体障害です。
BとCを比較すると、Bは嵩高いですがCはアルキル基が環状構造によって固定されているため、Cの方が立体障害が小さいと言えます。
したがって、塩基性はC > Bであり、全てをまとめると解答のようになります!
3. (ⅱ)
解答
C
アルキル基が環構造によって固定され、Nの孤立電子対周辺の立体障害が小さいため
解説
先ほどの問題とも関連してきますが、Cはアルキル基が孤立電子対の後ろで固定されているため電子がむきだしになっているような状態です。
したがって、Cは求核性が非常に高いため求核置換反応の反応速度は大きいということができます!
Ⅱ.
1. (ⅰ)
解答
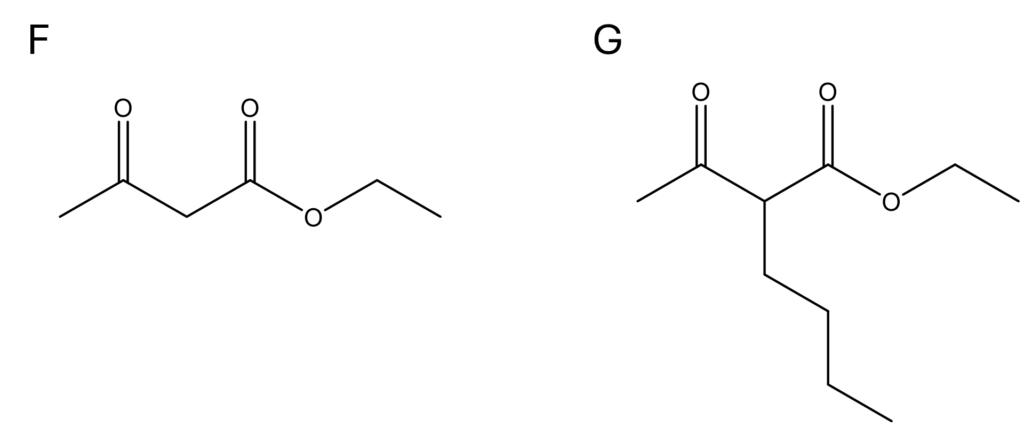
解説
fの合成反応はいわゆるClaisen縮合です。
塩基が脱離基と同じであることから、α炭素の反応であることに気がつきましょう!
まず、エステルのα水素がNaOEtによって引き抜かれ、エノラートイオン発生します。
そして、このエノラートがエステルのカルボニル基に攻撃し、アルコキシドが脱離することで解答のようなβ-ケトエステルが生成します。
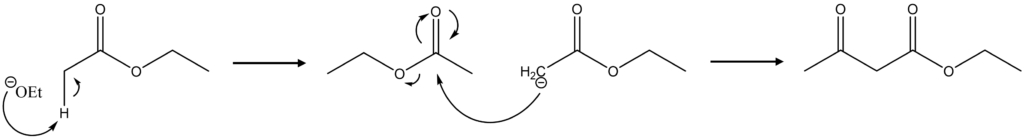
ちなみに、Claisen縮合では反応が終結した後に反応混合物にAcOHやHClなどの酸を加えます。
酸はβ-ケトエステルがアニオンになることを防いだり、生じたアルコキシドイオンをプロトン化して、逆反応が進むのを防ぐ役割を果たします。
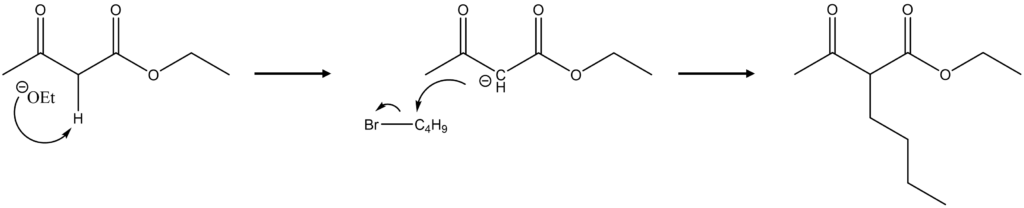
続いて、アルキル化が起こります。
同様にNaOEtによって、α水素が引き抜かれてエノラートイオンが生成します。
このうち、2つのカルボニル基に囲まれているα水素は容易に引き抜かれやすいです。
そして、このエノラートがハロゲン化アルキルに攻撃することで、Gのようなアルキル化されたβ-ケトエステルを得ることができます!
1. (ⅱ)
解答
解説
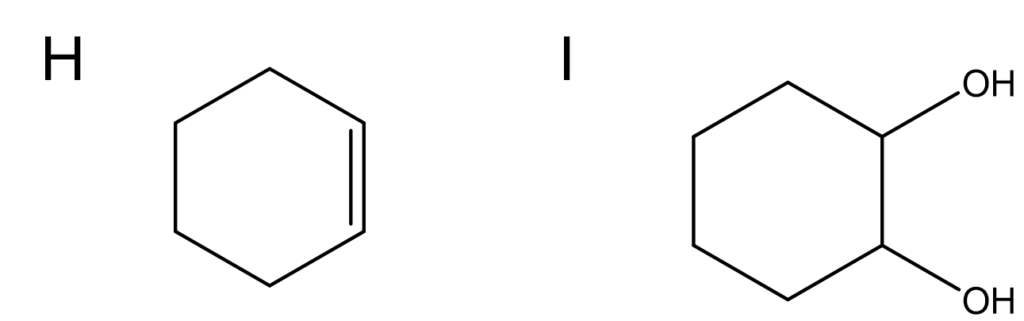
Hはジブロモ体のE2脱離反応です。
ヨウ化物イオンが一方の臭素に攻撃し、他方の臭素が脱離することによってシクロヘキセンが生成します。
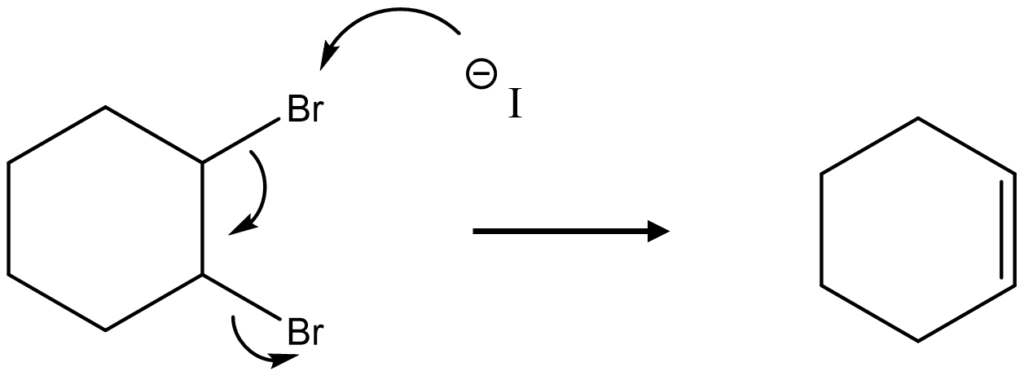
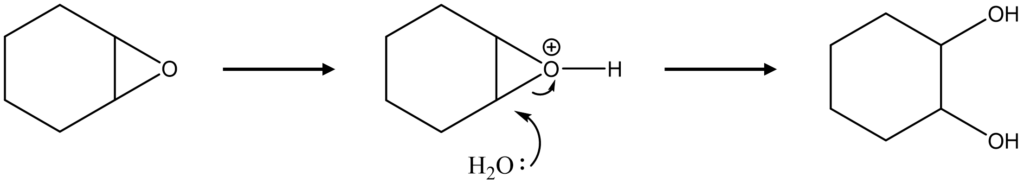
続いて、過ギ酸とシクロヘキサンが反応することによってエポキシドが生成し、これと酸条件下で水と反応することで解答のようなジオールが生成します。
1. (ⅲ)
解答
解説
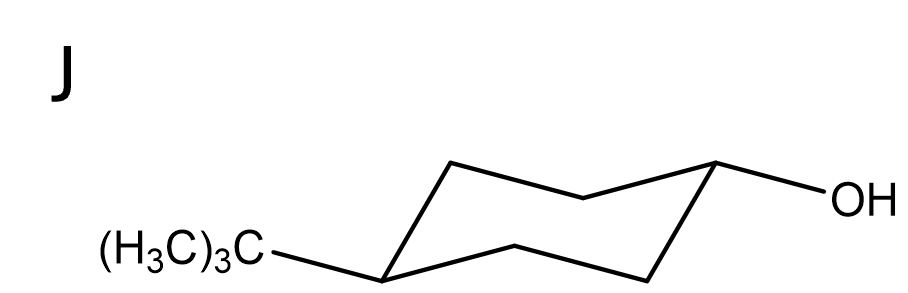
ケトンの還元反応です。
しかし、単純な反応ではなくシクロヘキサノンであることに注意が必要です!
endo方向とexo方向のいずれで近づくかによって、得られる立体異性体が異なります。
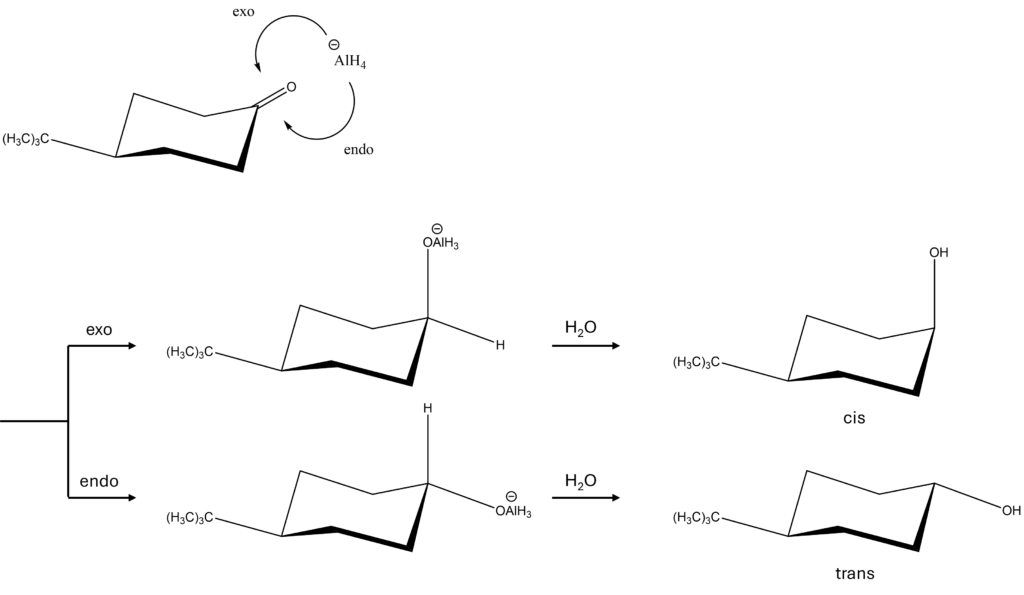
上図のように、endo方向から付加することによってより安定なtrans体が生成するので、これが解答となります!
2.
解答
(ⅰ)
(ⅱ)
まず、アントラニル酸のアミノ基と亜硝酸アミルでジアゾ化が起きて、図1のような化合物が得られる。そして、この化合物から脱炭酸とそれに続くN2の除去が生じることによって、Kが生成する。
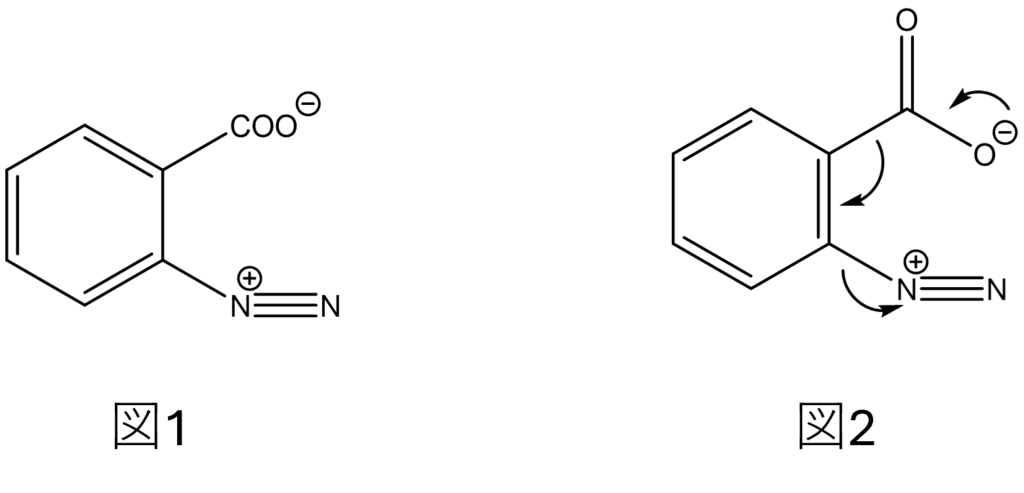
解説
今回の問題は、最終生成物が分かっているので逆合成解析によって反応物を考えていきましょう。
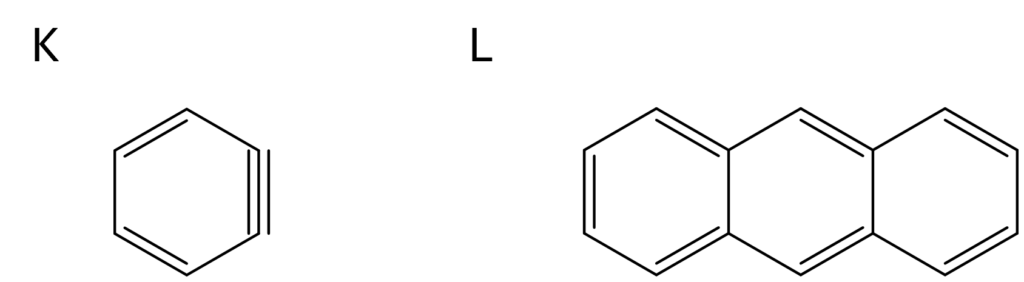
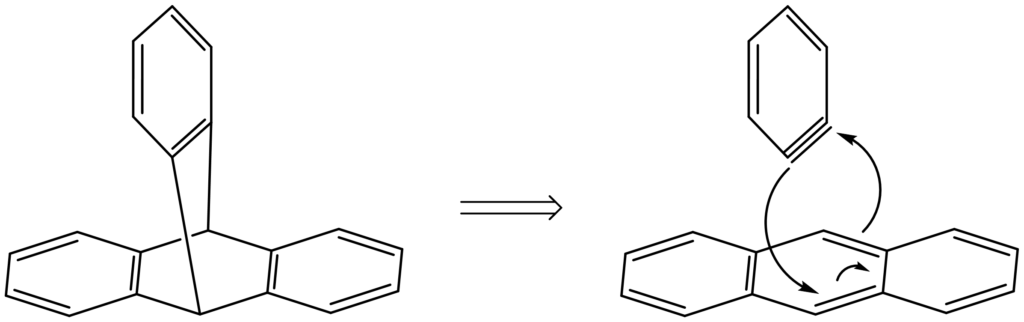
アントラニル酸は環が1つで、トリプチセンは環が複数あることからLは複数のベンゼン環からなる化合物、すなわちアントラセンではないかと予想できます。
ここで、2つのジエン(ベンゼン環)を結びつける反応としてパッと思いつきたいのが『Diels-Alder反応』です。
Diels-Alder反応と仮定すると、ベンザイン(K)とアントラキセン(L)を用いればトリプチセンが得られると分かります。
続いて、(ⅱ)を解くには亜硝酸アミルにNO2基がついていることから、ジアゾ化が起こることに気がつけるかどうかが重要です。
このことを念頭に、実際に反応を見ていきましょう!
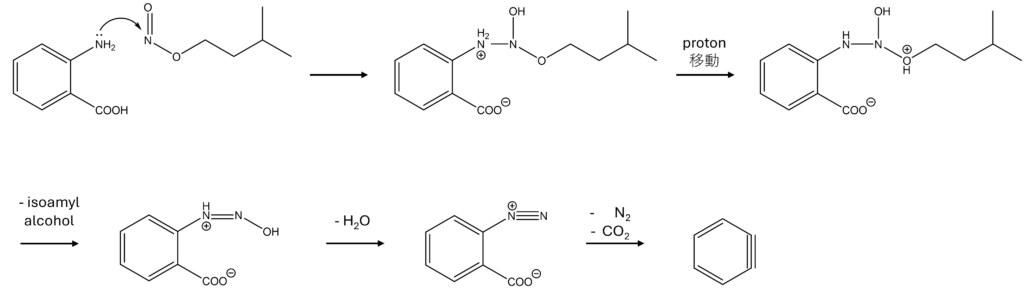
まず、アントラニル酸のアミノ基が亜硝酸アミルのNに攻撃することで、2分子が結合します。
そして、プロトンの移動とそれに続いてアルコールが脱離します。
最後に、H2Oが脱離することによってジアゾ化が進行します。
ジアゾ化の後、脱炭酸とそれに伴うN2の脱離が起こることによって、非常に不安定な(=反応性の高い)中間体であるベンザインが生成します。
トリプチセンは、このベンザインとアントラセンのDiels-Alder反応によって、合成することができます!
Ⅲ.
1.
解答
134 kJ mol-1
解説
問題に記載されている数値を図にすると、下図のようになります。

1,3-シクロヘキサジエンの水素化熱とシクロヘキセンの水素化熱の差である-110 kJ mol-1が、二重結合が1つ増えたときの水素化熱になります。
したがって、仮想の“シクロヘキサトリエン”の水素化熱は1,3-シクロヘキサジエンの水素化熱に-110 kJ mol-1を足した、
-230-110 =-340 kJ mol-1
が“シクロヘキサトリエン”の水素化熱です。
ベンゼンの水素化熱は-206 kJ mol-1であるため、この差がベンゼン環の共鳴安定化エネルギーです。
以上より、340-206=134 kJ mol-1が共鳴安定化エネルギーとなります!
2.
解答
M・N
Huckel則より、4n+2個(nは整数)のπ電子を持つとき芳香族性を有する。M・N・Lのπ電子数はそれぞれ10、18、20より、M・Nが芳香族性を有する。
解説
Huckel則に従うかどうかで判断できます。
Huckel則…π電子が4n+2個(nは整数)の場合、芳香族性を有する
解答のように、それぞれのπ電子数はそれぞれ10・18・20なので、MとNが芳香族性を有していることが分かります。
3.
解答
(ⅰ)
7員環側にカチオンが、5員環側にアニオンが分極した共鳴構造は芳香族性を有するため、寄与が大きい。したがって、大きな双極子モーメントを有する。
(ⅱ)
b
このような共鳴構造を有しており、bの位に負電荷が集中しているため。
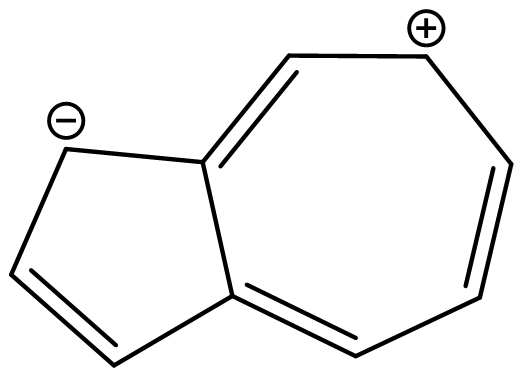
解説
アズレンの共鳴構造を描くと、下図のようになります。
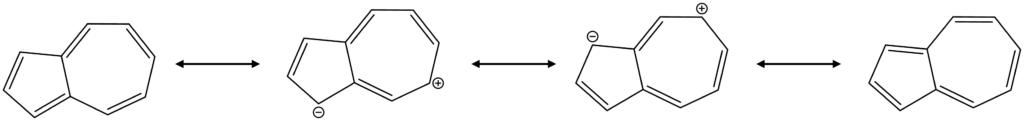
アズレンはこのように、分極した共鳴構造を有しています。
しかも、この電荷を有した共鳴構造は7員環と5員環ともに芳香族となります(π電子数が両方とも6個)。
したがって、この共鳴寄与体の影響が大きくなるため双極子モーメントも大きいと言えます!
また、共鳴構造から分かるようにbの位置に負電荷が集中しているため、この位置では容易に求電子置換が進むと予想されます。
最後に
いかがでしたか?
今回は、2024年度入学 東大院試 応用化学科 応用化学専攻の有機化学の問題について解説してきました。
今後も過去問の解説をどんどんしていきますので、ぜひ参考にしてみてくださいね!











コメント